学術・研究特設サイト
TOP > 学術・研究特設サイト > 治験審査委員会 > 神奈川県保険医協会の治験事業 先生も治験ネットワークに参加しませんか!
神奈川県保険医協会の治験事業 先生も治験ネットワークに参加しませんか!
開業医が治験を行う意義
 神奈川県保険医協会では、治験事業に取り組んでいます。治験というと「なんか難しいことをやっているな」とお考えの先生方もおられるかも知れません。しかし、現状では開業医の先生方が治験の担い手として期待が高まっているのです。
神奈川県保険医協会では、治験事業に取り組んでいます。治験というと「なんか難しいことをやっているな」とお考えの先生方もおられるかも知れません。しかし、現状では開業医の先生方が治験の担い手として期待が高まっているのです。
高血圧、高脂血症、糖尿病などの生活習慣病をもつ患者は年々増加しています。それに対する薬剤の開発もすすめられています。これまでは、治験を行うのは大学病院等の規模が大きいところで行われることが多かったのですが、生活習慣病患者を多く診ているのは開業医の先生方なので、治験の担い手として期待されているわけです。
治験は"大変"か?
そもそも治験を行うときには、患者へのインフォームドコンセントやカルテへのしっかりした記載など医療機関で実際に行われていることですが、更なる精度が求められます。しかし、ご安心下さい。実際治験を行う際には、CRCという治験コーディネーターが、派遣され、直接、患者さんにインフォームドコンセントのフォローをなど、先生の治験のお手伝いをすることになります。その意味では、先生は治験の計画書にしたがってすすめていただければよいのです。
治験を実際行うには?
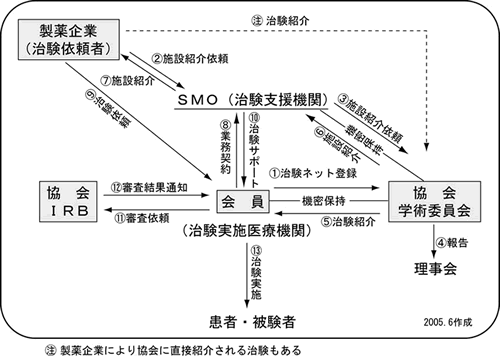
神奈川県保険医協会では、2003年に治験ネットワークを立ち上げました。関心のある先生は是非治験ネットワークにご登録いただきたいと思います。その際に先生と協会で機密保持契約を結ばせていただきます。これは、治験の情報を先生にお知らせするためです。また、SMOとも機密保持契約を結び、治験情報を協会に集中させています。そこで学術委員会で先生方が安心して参加できる治験かどうかチェックをし、治験ネットワークの先生方にお知らせしています。お知らせした治験情報の中から、関心がある先生には、アンケートをお答えいただき、製薬会社等の治験依頼者から訪問調査に行かせていただくことになります。
治験を行うための事前の準備(その1)
治験は厚生労働省の省令である「医薬品の臨床試験の実施の基準」(以下、GCP)に基づいて行う必要があります。これは薬事法に従うことが義務として盛り込まれています。
GCPには治験を実施する医療機関に「標準業務手順書」(以下、SOP)を設置することが義務付けられています。SOPは治験業務を誰が実施しても適切かつ均質に遂行できるように基本的な業務手順を体系的にまとめた手順書です。
このSOPについては、保険医協会で雛型を用意しています。これを早急に設置してください。
治験を行うための事前の準備(その2)
治験依頼者からの施設訪問を受け、治験依頼者から正式に治験を依頼された場合は、行う治験の計画について、審査を依頼する必要があります。その依頼する先を、「治験審査委員会」(以下、IRB)といいます。神奈川県保険医 協会ではIRBを2002年に設置しているので、申請書に基づき、申請していただくことになります。しかし、実際はSMOがお手伝いをしてくれますので、先生方は内容を確認していただければすすめることができます。
* 画像をクリックすると大きく表示
治験ネットワークに登録するには
治験に関心をもたれましたら、登録用紙をダウンロードいただき、FAX(045-313-2113 学術部担当宛)にてお申し込みください(アクセスの際には、 「会員ページ」と同じユーザー名、パスワードを入力する必要があります)。
そして最初に機密保持契約を結んでください。これにより、治験情報のご案内をさせていただくことができるようになります。
* 「会員ページ」と同じユーザー名、パスワードを入力
[重要]治験ネットワークへの登録は会員の医師・歯科医師に限らせていただきます。ご希望のかたはこの機会にぜひ保険医協会にご入会いただきますよう、よろしくご検討願います(入会に関するお問い合わせはこちら)。
【用語解説】
GCP(Good Clinical Practice/医薬品の臨床試験の実施の基準)
1997年3月27日厚生省令第28号により定められ、同年4月1日施行された、医薬品の臨床試験の実施の基準。
GCPは、被験者の人権と安全性の確保、臨床試験のデータの信頼性の確保をはかり、適正な臨床試験が実施されることを目的として定めた。
SMO(Site Management Organization/治験施設支援機関)
特定の医療機関(治験実施施設)と契約し、その施設に限定して治験業務を支援する機関(通常は、企業)のこと。
SOP(Standard Operating Procedures/標準業務手順書)
特定の業務を均質に遂行するために、その業務の手順について詳細に記述した指示書。治験業務を誰が実施しても適切かつ均質に遂行できるよう、基本的な業務手順を体系的にまとめた手順書のこと。
新GCPにおいては、治験に携わる、製薬メーカー(治験依頼者)、CRO、医療機関(治験実施施設)は、SOPを作成し、それに基づき作業を行うことが義務づけられている。
IRB(Institutional Review Board/治験審査委員会)
治験の依頼を受けた病院等の治験実施施設は、治験の実施において治験参加者の「人権」と「安全性」に問題ないかどうかを審査するための組織として、「IRB(治験審査委員会)」の設置を義務づけられている。IRBは、医学・科学の専門家及び非専門家によって構成される独立の(医療機関内、地域的、国立の)委員会となる。
IRBの責務は、特に、治験実施計画書とその改訂、並びに被験者から文書によるインフォームドコンセントを得るのに使用される方法及び資料(同意説明文書等)を審査し、承認し、また継続審査を行うことによって、被験者の人権、安全及び福祉の保護に対して公の保証を与えること。
IRBでは、治験参加者の人権と安全性を守るために、治験の依頼を受けた病院とは利害関係のない人や医薬専門外の人も加えて組織される。
CRC(Clinical Research Coordinator/治験コーディネーター)
「治験コーディネーター」(CRC)とは、治験実施施設にて治験責任医師または治験分担医師の指示のもと、治験の進行をサポートするスタッフの職種を指す。
インフォームドコンセントや同意説明、参加者の心のケアなどの、医学的判断を伴わない被験者に係わる業務や、治験が円滑に行われるように、治験(臨床試験)に係わる事務的業務、治験(臨床試験)に携わるチーム内の調整をする業務を担当する。
開業医が治験を行う意義
 神奈川県保険医協会では、治験事業に取り組んでいます。治験というと「なんか難しいことをやっているな」とお考えの先生方もおられるかも知れません。しかし、現状では開業医の先生方が治験の担い手として期待が高まっているのです。
神奈川県保険医協会では、治験事業に取り組んでいます。治験というと「なんか難しいことをやっているな」とお考えの先生方もおられるかも知れません。しかし、現状では開業医の先生方が治験の担い手として期待が高まっているのです。
高血圧、高脂血症、糖尿病などの生活習慣病をもつ患者は年々増加しています。それに対する薬剤の開発もすすめられています。これまでは、治験を行うのは大学病院等の規模が大きいところで行われることが多かったのですが、生活習慣病患者を多く診ているのは開業医の先生方なので、治験の担い手として期待されているわけです。
治験は"大変"か?
そもそも治験を行うときには、患者へのインフォームドコンセントやカルテへのしっかりした記載など医療機関で実際に行われていることですが、更なる精度が求められます。しかし、ご安心下さい。実際治験を行う際には、CRCという治験コーディネーターが、派遣され、直接、患者さんにインフォームドコンセントのフォローをなど、先生の治験のお手伝いをすることになります。その意味では、先生は治験の計画書にしたがってすすめていただければよいのです。
治験を実際行うには?
神奈川県保険医協会では、2003年に治験ネットワークを立ち上げました。関心のある先生は是非治験ネットワークにご登録いただきたいと思います。その際に先生と協会で機密保持契約を結ばせていただきます。これは、治験の情報を先生にお知らせするためです。また、SMOとも機密保持契約を結び、治験情報を協会に集中させています。そこで学術委員会で先生方が安心して参加できる治験かどうかチェックをし、治験ネットワークの先生方にお知らせしています。お知らせした治験情報の中から、関心がある先生には、アンケートをお答えいただき、製薬会社等の治験依頼者から訪問調査に行かせていただくことになります。
治験を行うための事前の準備(その1)
治験は厚生労働省の省令である「医薬品の臨床試験の実施の基準」(以下、GCP)に基づいて行う必要があります。これは薬事法に従うことが義務として盛り込まれています。
GCPには治験を実施する医療機関に「標準業務手順書」(以下、SOP)を設置することが義務付けられています。SOPは治験業務を誰が実施しても適切かつ均質に遂行できるように基本的な業務手順を体系的にまとめた手順書です。
このSOPについては、保険医協会で雛型を用意しています。これを早急に設置してください。
治験を行うための事前の準備(その2)
治験依頼者からの施設訪問を受け、治験依頼者から正式に治験を依頼された場合は、行う治験の計画について、審査を依頼する必要があります。その依頼する先を、「治験審査委員会」(以下、IRB)といいます。神奈川県保険医 協会ではIRBを2002年に設置しているので、申請書に基づき、申請していただくことになります。しかし、実際はSMOがお手伝いをしてくれますので、先生方は内容を確認していただければすすめることができます。
* 画像をクリックすると大きく表示
治験ネットワークに登録するには
治験に関心をもたれましたら、登録用紙をダウンロードいただき、FAX(045-313-2113 学術部担当宛)にてお申し込みください(アクセスの際には、 「会員ページ」と同じユーザー名、パスワードを入力する必要があります)。
そして最初に機密保持契約を結んでください。これにより、治験情報のご案内をさせていただくことができるようになります。
* 「会員ページ」と同じユーザー名、パスワードを入力
[重要]治験ネットワークへの登録は会員の医師・歯科医師に限らせていただきます。ご希望のかたはこの機会にぜひ保険医協会にご入会いただきますよう、よろしくご検討願います(入会に関するお問い合わせはこちら)。
【用語解説】
GCP(Good Clinical Practice/医薬品の臨床試験の実施の基準)
1997年3月27日厚生省令第28号により定められ、同年4月1日施行された、医薬品の臨床試験の実施の基準。
GCPは、被験者の人権と安全性の確保、臨床試験のデータの信頼性の確保をはかり、適正な臨床試験が実施されることを目的として定めた。
SMO(Site Management Organization/治験施設支援機関)
特定の医療機関(治験実施施設)と契約し、その施設に限定して治験業務を支援する機関(通常は、企業)のこと。
SOP(Standard Operating Procedures/標準業務手順書)
特定の業務を均質に遂行するために、その業務の手順について詳細に記述した指示書。治験業務を誰が実施しても適切かつ均質に遂行できるよう、基本的な業務手順を体系的にまとめた手順書のこと。
新GCPにおいては、治験に携わる、製薬メーカー(治験依頼者)、CRO、医療機関(治験実施施設)は、SOPを作成し、それに基づき作業を行うことが義務づけられている。
IRB(Institutional Review Board/治験審査委員会)
治験の依頼を受けた病院等の治験実施施設は、治験の実施において治験参加者の「人権」と「安全性」に問題ないかどうかを審査するための組織として、「IRB(治験審査委員会)」の設置を義務づけられている。IRBは、医学・科学の専門家及び非専門家によって構成される独立の(医療機関内、地域的、国立の)委員会となる。
IRBの責務は、特に、治験実施計画書とその改訂、並びに被験者から文書によるインフォームドコンセントを得るのに使用される方法及び資料(同意説明文書等)を審査し、承認し、また継続審査を行うことによって、被験者の人権、安全及び福祉の保護に対して公の保証を与えること。
IRBでは、治験参加者の人権と安全性を守るために、治験の依頼を受けた病院とは利害関係のない人や医薬専門外の人も加えて組織される。
CRC(Clinical Research Coordinator/治験コーディネーター)
「治験コーディネーター」(CRC)とは、治験実施施設にて治験責任医師または治験分担医師の指示のもと、治験の進行をサポートするスタッフの職種を指す。
インフォームドコンセントや同意説明、参加者の心のケアなどの、医学的判断を伴わない被験者に係わる業務や、治験が円滑に行われるように、治験(臨床試験)に係わる事務的業務、治験(臨床試験)に携わるチーム内の調整をする業務を担当する。
研究会開催予定
研究会開催予定の予定はありません
参加対象
- 会員会員と会員医療機関のスタッフ
- 医・歯すべての医師・歯科医師
- 従医療機関のスタッフ
- 一般一般の方
※神奈川県保険医協会が主催する全ての研究会等には、 (株)神保協が後援しております。